2023年4月19日《The Lancet》在线发表了DESTINY-Breast02研究的结果。TRAStuzumab deruxtecan versus treatment of physician's choice in patients with HER2-positive metastatic breast cancer (DESTINY-Breast02): a randomised, open-label, multicentre, phase 3 trial
pPJ帝国网站管理系统
德曲妥珠单抗是一种抗体偶联药物物,由人源化单克隆抗HER2抗体通过可裂解连接子结合到细胞毒性拓扑异构酶I抑制剂上。T-DXd在II期单臂DESTINY-Breast01试验中显示出强大的活性,该试验在先前接受T-DM1的且多线经治的HER2阳性乳腺癌患者中进行,达到61%的客观缓解率(184例患者中有112例),中位无进展生存期为16.4个月(12.7个月-不可估计[NE])。这些结果加速了德曲妥珠单抗用于HER2阳性转移性乳腺癌患者的批准,适应症患者之前至少接受过两种基于抗HER2抗体的方案。DESTINY-Breast01的最新结果继续显示T-DXd在T-DM1之后持续有效,患者的中位无进展生存期为19.4个月(14.1-25.0),中位总生存期为29.1个月(24.6-36.1),客观缓解率为62% (184例患者中114例)pPJ帝国网站管理系统
DESTINY-Breast02被设计为DESTINY-Breast01的验证性试验。研究的目的是比较T-DXd与医生选择治疗对T-DM1耐药或难治的HER2阳性转移性乳腺癌患者的疗效和安全性。
pPJ帝国网站管理系统
背景:在单臂II期Destiny-Breast01试验中,T-DXd在T-DM1难治或耐药,缺乏有效治疗的HER2阳性转移性乳腺癌患者中显示出强大的活性(robust activity)。DESTINY-Breast02的目的是比较T-DXd与医生选择的治疗在该患者群体中的疗效和安全性。pPJ帝国网站管理系统
方法:这项随机、开放标签、多中心、III期试验在北美、欧洲、亚洲、澳大利亚、巴西、以色列和土耳其的227个地点(医院、大学医院、诊所、社区中心和私立肿瘤中心)进行。符合条件的患者年龄为18岁或以上,患有不可切除或HER2阳性转移性乳腺癌,先前接受过T-DM1治疗,疾病进展,ECOG评分为0或1,肾功能和肝功能正常。患者被随机分配(2:1)接受T-DXd(静脉注射剂量为5.4 mg/kg,每3周1次)或采用分组随机法接受医生选择的治疗。医生选择的治疗方法是卡培他滨(1250 mg/m2;每天口服2次,第1- 14天)加曲妥珠单抗(第1天静脉注射8mg /kg,然后每天一次6mg /kg)或卡培他滨(1000mg /m2)加Apatinib/ target=_blank class=infotextkey>LApatinib/ target=_blank class=infotextkey>拉帕替尼(1250mg口服,每天一次,第1- 21天),疗程21天。主要终点是基于全分析集的盲法独立中心评价的无进展生存期。ClinicalTrials.gov:NCT03523585。pPJ帝国网站管理系统
发现:在2018年9月6日至2020年12月31日期间,608名患者被随机分配接受T-DXd治疗(n=406;2例未接受治疗)或医生选择的治疗(n=202;7人未接受治疗)。608例(100%)患者被纳入完整分析集。T-DXd组的中位年龄为54.2岁(IQR 45.5-63.4),医生选择治疗组的中位年龄为54.7岁(48.0-63.0)。
白人384例(63%),女性603例(99%),男性5例(<1%)。
pPJ帝国网站管理系统
T-DXd组的中位随访时间为21.5个月(IQR为15.2-28.4),医生选择治疗组的中位随访时间为18.6个月(8.8-26.0)。
经盲法独立中心评价,T-DXd组的中位无进展生存期为17.8个月(95% CI 14.3-20.8),而医生选择治疗组的中位无进展生存期为6.9个月(5.5-8.4)(HR 0.36 [0.28-0.45];p < 0.0001)。pPJ帝国网站管理系统
恶心(T-DXd组404例中有293例[73%],医生选择治疗组195例中有73例[37%])
手掌-足底红肿综合征(7例[2%]vs100例[51%])。
接受T-DXd治疗的患者中有213例(53%)发生了3级或更高级别的治疗不良事件,而接受医生选择治疗的患者中有86例(44%)发生了3级或更高级别的治疗不良事件;而药物相关性间质性肺疾病发生率为42例(10%;包括2例5级死亡事件)vs 1例(<1%)。
经盲法独立中心评价,T-DXd组的中位无进展生存期为17.8个月,而医生选择治疗组的中位无进展生存期为6.9个月(5.5-8.4)(HR 0.36 p < 0.0001;图2 a)。
在12个月时,T-DXd治疗组无疾病进展的患者比例为62.3%(57.0-67.1),而医生选择治疗组为27.2% (20.1-34.8);而在24个月时,42.2%(36.5-47.8)对13.9%(7.9-21.6)。
预先指定的亚组分析显示,通过盲法独立中心评价,在所有亚组中,T-DXd的无进展生存优于医生选择的治疗,无论激素受体状态、既往用帕妥珠单抗治疗、内脏疾病史和基线时脑转移(图2B)。pPJ帝国网站管理系统
T-DXd组的中位总生存期为39.2个月,而医生选择治疗组的中位总生存期为26.5个月(HR 0.66 [0.50-0.86];p = 0.0021;图3)。治疗组间总生存期差异跨越边界,本分析差异为0.0040,具有统计学意义。
T-DXd组12个月生存率为89.4%(85.9-92.1),而医生选择治疗组为74.7% (67.6-80.4);而在24个月时,相应的百分比为65.9%(60.7-70.7)和54.3%(46.3-61.6)。pPJ帝国网站管理系统
通过盲法独立中心评价,客观缓解率为:接受T-DXd治疗406例患者中有283例(70%),接受医师选择治疗202例患者中有59例29%,图4;
T-DXd组57例(14%)患者达到完全缓解,医生选择治疗组10例(5%)患者达到完全缓解,
226例(56%)患者达到部分缓解,49例(24%)患者达到部分缓解。
在T-DXd治疗组中,19例(5%)患者出现了进展性疾病,而在医生选择治疗组中,26例(13%)患者疾病进展。
研究者评估的两个治疗组的客观反应与盲法独立中心回顾评估的反应相似。T-DXd治疗的中位反应持续时间为19.6个月(95% CI 15.9-NE),而医生选择的治疗的中位反应持续时间为8.3个月(5.8-9.5)。研究者评估的中位无进展生存期:T-DXd组为16.7个月(14.3-19.6),而医生选择治疗组为5.5个月(4.4-7.0)(HR 0.28 [0.23-0.35];p < 0.0001;)。每个方案分析集中的无进展生存数据与完整分析集中一致。
图4:T-DXd的抗肿瘤活性(A)和医生选择的治疗方法(B)
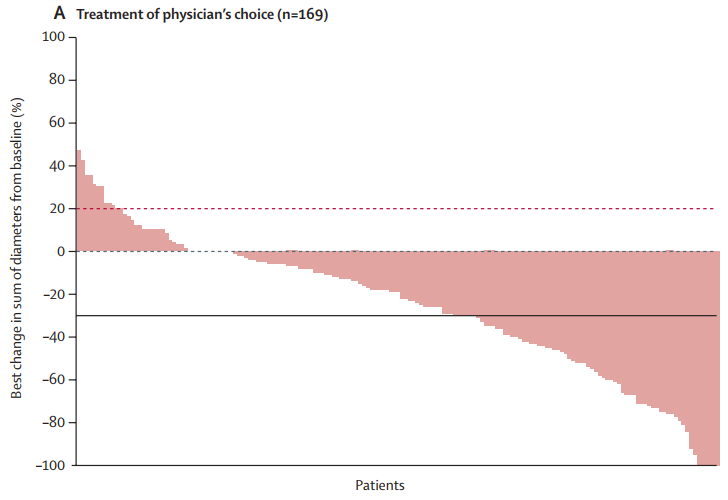 pPJ帝国网站管理系统
pPJ帝国网站管理系统
对于探索性疗效终点,6个月临床获益率为82% (406例患者中有334例)使用T-DXd,医生选择的治疗:46% (202例患者中有93例(附录p 2),中位无进展生存期2为35.8个月(28.4 ne)对15.8个月(13.5-21.0;Hr 0.45[0.34-0.59])。
在停止研究治疗的患者中,T-DXd组310例患者中有220例(71%),医生选择组190例患者中有140例(74%)在试验后接受了全身癌症治疗。T-DXd组的全身癌症治疗包括曲妥珠单抗(310例中126例[41%])、T-DXd组(18例[6%])、T-DM1(3例[<1%])、抗HER2酪氨酸激酶抑制剂(124例[40%])、其他全身治疗(188例[61%])。在医生选择治疗组,190例患者中有94例(49%)接受曲妥珠单抗治疗,52例(27%)接受T-DXd治疗,5例(3%)接受T-DM1治疗,42例(22%)接受抗HER2酪氨酸激酶抑制剂治疗,107例(56%)在停止研究治疗后接受其他全身治疗。
T-DXd治疗的中位持续时间为11.3个月(IQR 6.2-20.5),医生选择的治疗约为4.5个月(曲妥珠单抗4.4个月[2.5-8.7],卡培他滨4.6个月[2.1-8.9],Lapatinib/ target=_blank class=infotextkey>拉帕替尼4.5个月[2.1-10.6])。
404例接受T-DXd治疗的患者中,403例发生了任何级别的治疗严重不良事件,195例接受医生选择的治疗中,185例(95%)发生了3级或以上的治疗严重不良事件,213例(53%)对86例(44%)。接受T-DXd治疗的患者中,394例(98%)报告了药物相关的治疗严重不良事件,167例(41%)发生了3级或以上的药物相关事件。在任何级别(0.85 vs 1.66)和3级或更高级别(0.45 vs 0.77)的治疗不良事件方面,接受T-DXd治疗的患者的暴露调整发生率低于接受医生选择治疗的患者。
404例接受T-DXd治疗的患者中有58例(14%)出现药物相关治疗不良事件,195例接受医生选择治疗的患者中有10例(5%)出现药物相关治疗不良事件。与停药相关的最常见治疗不良事件使用T-DXd:肺炎(25例[6%])和间质性肺疾病(15例[4%]),医生选择的治疗:掌足底红肿(3例[2%])。在接受T-DXd治疗的患者中,出现了132例(33%)与药物中断相关的药物相关治疗不良事件,而接受医生选择治疗的患者中出现了76例(39%);而与剂量减少相关的患者有95人(24%)比89人(46%)。T-DXd组有4例(<1%)患者报告了药物相关治疗出现的与死亡相关的不良事件(2例为肺炎,1例为急性髓性白血病,1例为肺炎),而医生选择治疗组无此类事件。
最常见的任何级别治疗中出现的不良事件(两组患者均≥15%)是恶心(T-DXd组404例中有293例[73%],医生选择治疗组195例中有73例[37%])、呕吐(152例[38%]对25例[13%])、脱发(150例[37%]对8例[4%])、疲劳(147例[36%]对52例[27%])、腹泻(109例[27%]对105例[54%])和手掌-足底红肿(7例[2%]对100例[51%];最常见的3级或以上治疗不良事件是中性粒细胞计数下降(T-DXd组为43例[11%],医生选择治疗组为4例[2%])、贫血(32例[8%]对6例[3%])、中性粒细胞减少(31例[8%]对4例[2%])、恶心(27例[7%]对5例[3%])、掌足底红肿(1例[<1%]对20例[10%])和腹泻(11例[3%]对14例[7%])。
最常见的治疗中出现的最严重毒性等级的不良事件见附录(第8页)。在研究开始时,不推荐使用止吐药;然而,该协议后来被修改(版本5;2020年4月23日),包括患者接受T-DXd前预防性止吐治疗的建议。在研究治疗期间,T-DXd组292例(72%)患者和医生选择治疗组60例(31%)患者接受了止吐药。在T-DXd组中,79例(20%)患者出现两次以上恶心发作,而医生选择治疗组为2例(<1%),30例(7%)患者出现两次以上呕吐,而非1例(<1%)。
启示:DESTINY-Breast02显示了T-DXd在HER2阳性转移性乳腺癌患者中的有利获益-风险特征,正如之前在DESTINY-Breast01中报道的那样,并且是第一个显示一种抗体偶联药物偶联物可以克服对前面ADC药物耐药性的随机研究。pPJ帝国网站管理系统
HER2阳性转移性乳腺癌患者对T-DM1难治或耐药,治疗选择很少。在最后一名患者随机分配后的18个月,我们观察到T-DXd与医生选择的治疗相比,中位无进展生存期(通过盲法独立中心评价)改善了10.9个月。医生选择治疗组的总体疗效结果与先前使用类似化疗方案的研究一致或更好,而T-DXd治疗的无进展生存期较医生选择治疗具有统计学意义和临床意义的改善。在所有预先指定的亚组中,T-DXd与医生选择的治疗相比,显示出一致的无进展生存获益,包括随机分层因素(激素受体状态、既往使用帕妥珠单抗治疗、内脏疾病史)和基线脑转移的存在。盲法独立中心评价的无进展生存期和研究者对曲妥珠单抗与医生选择的治疗的评估在我们的研究中是一致的,证实了研究者对肿瘤反应的充分评估。pPJ帝国网站管理系统
T-DXd对总生存率的改善也具有统计学意义和临床意义,与医生选择的治疗相比,死亡风险的HR为0.66。总体生存曲线在6个月左右出现早期分化,12个月时绝对改善14.7%。与医生选择的治疗相比,T-DXd的中位总生存期提高了12.7个月。在医生选择治疗组中,大约27%停止研究治疗的患者在试验后继续接受T-DXd,这可能有助于医生选择治疗显示的中位总生存期。未来的长期随访分析应该探索不同患者亚组的总体生存获益。pPJ帝国网站管理系统
经证实,T-DXd治疗的客观缓解率明显高于医生选择的治疗,而且中位缓解持续时间也明显更长。接受T-DXd治疗的患者中,14%的患者完全缓解为最佳缓解,而接受医生选择治疗的患者中,这一比例为5%。T-DXd治疗组停止治疗的患者少于医生选择治疗组(77%对97%),在初步分析中,23%对3%的患者仍在接受治疗;大多数停药与疾病进展有关。总的来说,更多的患者由于不良事件(18%对7%的医生选择治疗)和患者停药(7%对9%)而停止使用T-DXd治疗。对这一人群的治疗结果进行进一步分析可能是有必要的。总的来说,与接受医生选择治疗的患者相比,接受T-DXd治疗的患者治疗时间更长,客观缓解率更高,反应持续时间更长,无进展生存期更长,总生存期更长。研究治疗后的下一条治疗线的疾病进展或死亡(无进展生存期2)强烈倾向于T-DXd组,由于该分析的无进展生存期2数据成熟度较低,未来的分析将提供更清晰的信息。pPJ帝国网站管理系统
考虑到交叉试验比较应该谨慎解释,T-DXd在Destiny-Breast 02中观察到的临床疗效结果在数字上高于目前治疗方案中观察到的在两种或两种以上抗HER2治疗后进展的HER2阳性转移性乳腺癌患者。其他HER2靶向治疗的中位无进展生存期(如T-DM1 [TH3RESA试验],Margetuximab [SOPHIA试验],tucatinib [HER2CLIMB试验]和neratinib [NALA试验]),先前的PFS范围为5.6至7.8个月;中位总生存期为21.0 ~ 22.7个月,客观缓解率为22.0% ~ 40.6%。pPJ帝国网站管理系统
本研究中T-DXd的总体安全性与该药的既定安全性一致,未观察到新的安全性信号。尽管治疗组之间药物相关和非药物相关治疗出现的不良事件发生率相似,但与医生选择的治疗相比,T-DXd治疗中与停药相关的治疗出现的不良事件发生率更高(14%对5%)。暴露调整的发生率,即治疗组间中位治疗持续时间的差异,在任何级别和3级或更高级别的治疗中出现的不良事件,T-DXd治疗比医生选择的治疗更低。DESTINY-Breast02正在评估患者报告的结果,以衡量T-DXd治疗与医生选择的治疗对生活质量的影响。pPJ帝国网站管理系统
在T-DXd组中,最常见的任何级别治疗中出现的不良事件本质上是胃肠道。在两个治疗组中,相当数量的患者服用了止吐药,这可能减少了复发性恶心和呕吐事件的频率。然而,考虑到T-DXd组中20%的患者仍然有两次或两次以上恶心发作,7%的患者有两次或两次以上呕吐发作,早期用T-DXd治疗的止吐预防可能会进一步减少这些治疗引起的不良事件的发生。pPJ帝国网站管理系统
间质性肺病是与T-DXd治疗相关的重要风险。在本的研究中,确定的药物相关性间质性肺疾病发病的中位时间为29.9周。与DESTINY-Breast01相比,DESTINY-Breast02中药物相关的5级间质性肺疾病的发生率较低(2例[<1%]vs 5例[3%]),两项研究均未发生4级事件。在Destiny-Breast 01试验期间纳入了间质性肺疾病或肺炎的治疗指南,并在整个研究过程中进行了随访。目前的管理指南建议密切监测患者间质性肺疾病或肺炎的体征和症状,立即积极使用皮质类固醇治疗所有可疑事件,并延迟或停用T-DXd。这些修订后的指南可能解释了DESTINY-Breast02中观察到的5级间质性肺疾病或肺炎事件的数字发生率低于DESTINY-Breast01的原因。应该支持进一步的研究来探索间质性肺疾病的机制,并更好地识别和描述最危险的患者群体。我们认为,在常规临床实践中广泛应用T-DXd治疗乳腺癌应该提供更多的有效性和安全性数据,包括间质性肺疾病或肺炎,这可以在大型观察性研究和现实世界数据中进行评估。这项回顾性、观察性的DESTINY-Respond研究将探索T-DXd治疗HER2阳性和HER2低转移性乳腺癌(包括间质性肺疾病或肺炎)患者的有效性和安全性的真实数据。pPJ帝国网站管理系统
研究纳入了临床稳定、无症状的脑转移患者(两个治疗组在基线时均有18%的脑转移)。与医生选择的治疗相比,该亚组显示T-DXd的无进展生存期有临床意义的改善。未来对基线脑转移患者亚组的详细治疗和生存结果的探索性研究正在计划中。我们研究的一个局限性是排除了有症状或临床活跃的脑转移患者。另一个限制是医生选择组的治疗仅限于卡培他滨加曲妥珠单抗或拉帕替尼,尽管许多与其他化疗药物和HER2导向药物的联合策略在过去几年中被批准用于HER2阳性转移性乳腺癌患者的后期治疗。之所以选择卡培他滨,是因为在这种情况下,含卡培他滨的方案处方最多;然而,我们使用T-DXd的结果不能直接与含非卡培他滨化疗药物的方案或其他HER2定向药物的方案进行比较。在T-DXd被批准为HER2阳性转移性乳腺癌患者的二线治疗选择之前,T-DM1是该情况下的指南推荐治疗目前,基于DESTINY-Breast03的疗效和安全性结果,T-DXd是这些患者推荐的二线治疗pPJ帝国网站管理系统
DESTINY-Breast02的研究结果显示,T-DXd在HER2阳性转移性乳腺癌患者中对T-DM1耐药或难治的获益风险特征,如先前在DESTINY-Breast01中报道的那样,并支持该药作为T-DM1患者的首选治疗药物。据我们所知,这项研究是首个显示一种抗体偶联药物治疗在另一种抗体偶联药物治疗进展的患者中有显著益处的随机试验,为序贯抗体偶联药物治疗改善HER2阳性转移性乳腺癌患者和其他患者群体的疾病结局提供了乐观的前景。
内容来源:https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(23)00725-0/fulltext
























































